이하선에 고립되어 발생한 말초 거대세포 육아종 1예
A Case of an Isolated Peripheral Giant Cell Granuloma in the Parotid Gland
Article information
Trans Abstract
Peripheral giant cell granuloma (PGCG) is an benign non-neoplastic lesion most commonly occurring in oral cavity but extraoral PGCG is extremely rare. Recently, we experienced a case of an isolated PGCG in the parotid gland in 59-year-old man. FNAB findings and radiologic findings including CT and US were suggestive of Warthin’s tumor. Partial parotidectomy was performed. Pathologic findings showed fibrillar connective tissue stroma with spindled, ovoid, and round histiocytes-like cells mixed with uneven multinuclear giant cells, small capillaries, hemorrhage, hemosiderin-laden macrophages, and necrosis which were consistent with giant cell granuloma. We report a case of an PGCG in parotid with a review of literature.
서론
거대세포육아종(Giant cell granuloma)은 악골에서 주로 발생하는 중심 거대세포육아종(Central giant cell granuloma)과 구강내 연조직에서 주로 발생하는 말초 거대세포육아종(Peripheral giant cell granuloma)으로 분류되는 비신생성(non-neoplastic) 병변이다. 주로 악골의 골 내에 발생하는 비신생성 섬유-골화성 병변(fibro-osseous lesion)인 중심 거대세포육아종과 달리, 말초 거대세포육아종의 경우 주로 구강 내 반복적인 국소 자극이나 외상에 반응하여 치주인대나 골막에서 유래하는 것으로 추정되며, 구강 외에서 발생하는 경우가 매우 드물고, 발생하더라도 주변 골조직과의 연관을 가진다. 저자들은 최근 주변 골조직과 연관없이 이하선에 단독으로 발생한 말초 거대세포육아종 1예를 경험하여 문헌고찰과 함께 보고하고자 한다.
증례
59세 남자 환자가 4주 전부터 우측 귀 아래 생긴 종괴를 주소로 내원하였다. 종괴는 크기의 변화는 없었으나 1주 전부터는 불편감을 유발하였다고 하였다. 환자는 고혈압 및 갑상샘 저하증, 우울증으로 경구 약제를 복용 중이었고 하루 1갑씩, 20년간의 흡연력이 있었으며 우측 귀 아래쪽으로 외상이나 자극이 될만한 과거력은 없었다. 신체검사상 우측 귀 밑 이하선 부위에 직경 약 1cm 크기의 원형의 종괴가 촉진되었다. 종괴는 주변 조직과 유착 소견은 없이 가동성을 보였으며 종괴를 덮고 있는 피부에도 이상 소견은 관찰되지 않았다. 또한 안면신경 마비의 징후는 관찰되지 않았다 경부 초음파 검사 상직경 1.03×0.86 cm 크기의 저음영을 보이는 종괴가 관찰되었고(Fig. 1), 세침흡인생검에서 괴사조직을 동반한 다핵거대세포와 비정형 호산과립세포(Oncocytic cell)가 관찰되었으며 악성세포는 관찰되지 않았다(Fig. 2). 경부 컴퓨터단층촬영 검사에서 우측 이하선 천엽에 약 1.0 × 0.9 cm 크기의 낭성 종괴가 관찰되었고 종괴의 주변 부위는 초기 조영 증강 및 지연 조영감쇄(Washout enhancement) 양상을 보여 와르틴 종양(Warthin’s tumor)이 의심되었다(Fig. 1).

Preoperative CT and Ultrasonography findings. An approximate 1.0×0.9 cm-sized cystic lesion with peripheral enhancement and washout enhancement pattern was observed on axial (A) and coronal (B) CT images. An approximate 1.03×0.86 cm-sized hypoechogenic mass was observed on US images (C).
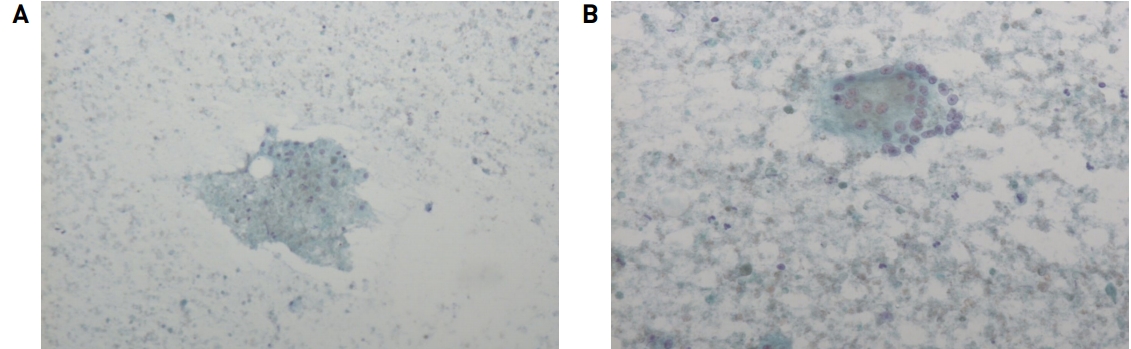
FNAB findings. A few atypical oncocytic cells (A, ×200), a few multinucleated giant cells and atypical oncocytic cells (B, ×200) in the necrotic background were suggestive of Warthin’s tumor.
이에 이하선 부분절제술을 시행하였다. 변형 Blair 절개를 시행한 후 종괴 및 주변 정상 이하선 조직을 포함한 이하선 부분절제술을 시행하였다. 종양은 우측 이하선의 천엽에 위치하였고 심측으로 안면신경의 가지 및 천측으로 대이개신경의 후방주행 가지와 접하고 있었다. 수술 중 안면신경은 보존하였으며 대이개신경의 후방주행 가지의 일부는 종괴와 함께 절제하였다. 종괴는 주변 조직과 약간의 유착 소견을 보였으나 비교적 뚜렷한 경계를 보여 주변 이하선 조직의 일부를 포함하여 완전 적출이 가능하였고, 절제된 수술검체 크기는 5.5 × 2.8 × 2.2 cm 이었다.
조직학적 검사 결과 섬유성 결합 조직 버팀질 내 방추형, 타원형 혹은 원형의 조직구 형태의 세포가 불규칙한 다핵거대세포와 섞여 있고, 작은 모세혈관 및 부분 출혈 소견, 헤모시데린이 침착된 대식세포, 부분 괴사 소견이 관찰되었다(Fig. 2). 면역조직화학염색 결과 CD68 염색에 양성 (Fig. 3), Ki-67 염색에는 1% 미만으로 낮은 양성율을 보였다. 이상의 종괴의 위치, 조직병리학적 소견 및 면역조직화학염색 결과를 종합하여 세포 증식의 정도가 낮은 양성의 말초 거대세포육아종으로 최종 진단되었다.
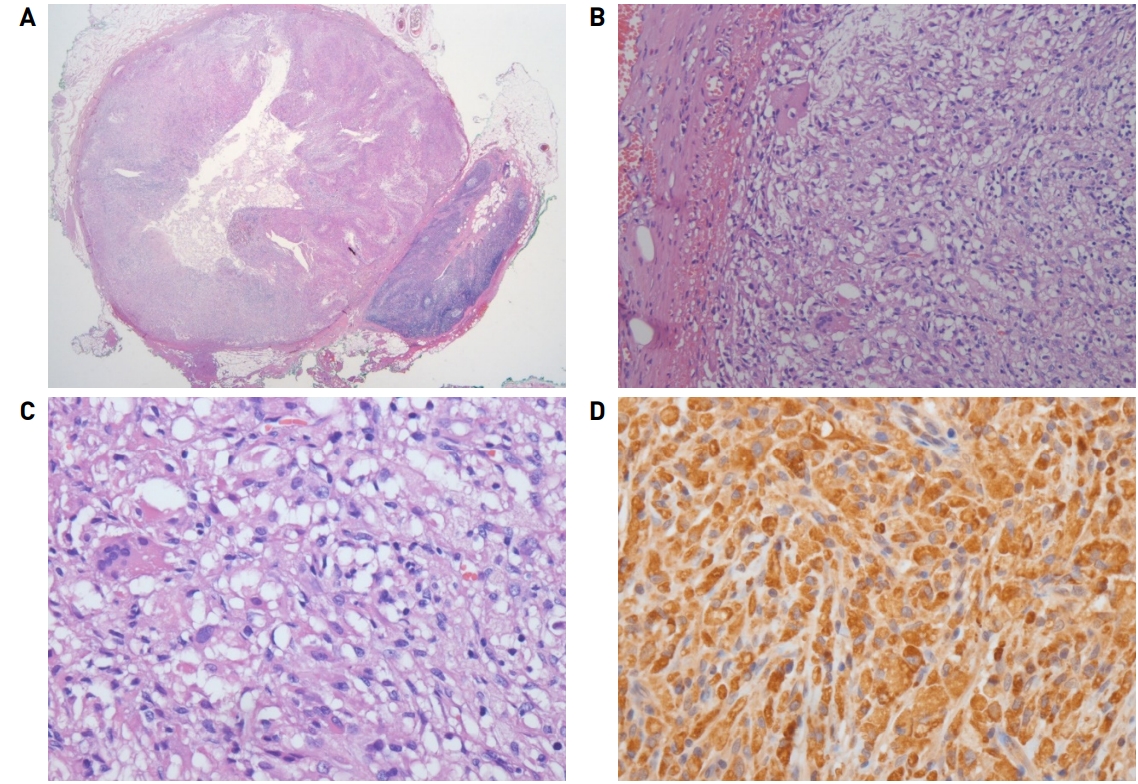
Histopathologic and Immunohistochemical findings. (A) Giant cell granuloma was noticed on scan view. Fibrillar connective tissue stroma mixed with uneven multinuclear giant cells, small capillaries, hemorrhage, hemosiderin-laden macrophages, and necrosis (D, ×200), multinucleated giant cells and intervening spindled, ovoid, and round histocytes-like cells (C, ×400) were noticed. (H&E stain) The immunohistochemical stain for CD68 shows diffuse positive in histiocytes (D, ×400).
환자는 수술 직후에는 안면신경 마비가 없었으나, 수술 다음 날 경미한 하악신경 마비의 징후를 보였고 술 후 3주 간의 외래추적관찰 기간 동안 호전되었으며 이차감염, 재발의 소견 없어 말초 거대세포육아종의 특성을 감안하여 1년 후 경부 컴퓨터단층촬영 시행하여 재발 여부에 관한 추적 관찰 예정이다.
고찰
거대세포육아종은 1952년 Jaffe에 의해 거대세포 수복성 육아종 (Giant-cell reparative granuloma)라는 명칭으로 처음 기술되었고, 엄밀히는 신생물(neoplasm)이 아니라 외상이나 골내 출혈이 발생한 병변의 국소적 수복 반응에 의해 형성된 덩이(mass)를 의미하였다[1,2]. 그러나 특별한 외상력이나 출혈, 자극이 없어도 발생이 가능하여 수복성이라는 명칭은 최근들어 사용하지 않는 추세이다[2,3,4]. 거대세포육아종은 버팀질 내 섬유모세포(Fibroblast)와 다핵거대세포의 증식이 관찰되는 종물로, 중심 거대세포육아종과 말초 거대세포육아종로 분류한다. 말초 거대세포육아종은 구강 내 국소적 자극이나 외상에 반응하여 치주인대 혹은 점막골막에서 유래하여 잇몸에 종물 형태로 나타나는 흔한 연조직 병변이나[5,6], 구강 외에서 발생하는 경우는 극히 드물고 뼈에 부착되어 있지 않은 점막에서는 발생한 예가 없다[6,7,8]. 중심 거대세포육아종은 주로 악골의 골내에 발생하는 비신생성 섬유-골화성 병변으로, 말초 거대세포육아종에 비해 빠른 성장, 높은 재발률, 골 재흡수 및 파괴로 인한 피질골 결손 등 좀 더 공격적인 특징을 보인다[6,9]. 본 증례의 경우 연조직에서 발생한 병변이므로 말초 거대세포육아종에 해당하나, 골 및 점막골막과 관계없이 이하선 내 고립되어 발생한 최초의 경우에 해당한다.
거대세포육아종은 주로 30대 미만의 연령에서 호발하는 것으로 알려져 있고 남성보다는 여성에서의 발병률이 높은 것으로 알려져 있으나[2,4,10] 말초 거대세포육아종의 경우 30대~50대에서 호발한다는 보고도 있다[6,11]. 악성화 또는 병변 주변으로의 공격적 전이의 특성은 보고된 바가 없다[4]. 본 증례는 평균적인 발생 연령보다 약간 고령의 남성에서 발생한 드문 증례이다.
거대세포육아종의 영상학적 소견은 비특이적이나, 컴퓨터단층촬영 상 출혈 또는 낭성 부분을 포함하는 불균질한 음영의 연조직 종괴로 나타날 수 있고, 공격적인 골미란 소견을 동반할 수 있다[10]. 본 증례의 경우 악골과는 분리된 단독 병변으로, 골 병변은 보이지 않았고 병변의 주변부에 조영증강을 보이는 낭성 종괴 소견을 보였다.
본 증례의 경우 초음파 유도하 시행한 세침흡인세포검사 상 괴사조직을 동반한 다핵거대세포와 비정형 호산과립세포가 관찰되어 영상학적 소견과 더불어 와르틴 종양을 의심하였다. 와르틴 종양의 경우 이하선에서 발생하는 2번째 흔한 양성 종양으로, 세침흡인세포검사 상 호산과립세포와 림프구가 모두 관찰될 경우 진단할 수 있어 본 증례의 검사 결과와 일치하지 않으나, 와르틴 종양의 경우 세침흡인세포검사 상 다핵거대세포가 발견되는 예가 있고[12], 호산과립세포가 관찰되는 질환의 호발 빈도를 고려하여 와르틴 종양을 의심하였다.
거대세포육아종은 조직병리학적으로 섬유성 결합 조직 버팀질 내 타원형 및 방추형의 단핵구와 모세혈관이 관찰되고, 모양과 크기가 다양한 다수의 다핵거대세포가 불규칙적으로 분포하며, 군데군데 출혈 소견 및 단핵구 내 헤모시데린 침착이 특징적이다. 또한, 신생 골형성 및 유골 조직을 둘러싼 뼈모세포가 고빈도로 관찰된다[3,5,13]. 말초 거대세포육아종과 중심 거대세포육아종은 조직병리학적으로 유사한 소견을 보이지만[5], 생물학적 특성에 차이를 보이고 있어 원인 규명을 위한 다양한 면역조직화학염색 연구가 이루어지고 있다.
면역조직화학염색 상 모든 다핵거대세포는 특징적으로 CD68 염색에 양성을 보이므로 염색의 양성 여부 및 양상으로 거대세포를 포함하고 있는 다른 종류의 병변이나 악성 종양과의 감별이 어느 정도 가능하다. 그러나 거대세포육아종의 병인과 발병기전, 말초 거대세포육아종과 중심 거대세포육아종의 차이의 원인에 관해서는 밝혀진 바가 많지 않은 상태로, 거대세포육아종을 구성하는 다핵거대세포의 기원이 파골세포 계통인지 단핵구-대식세포 계통인지 및 그 역할을 규명하기 위한 연구들이 있다[2,3,9,14]. 거대세포육아종을 구성하는 단핵구의 경우, 조직병리학적으로나 면역조직화학염색 상 다핵거대세포와 거의 유사한 특징을 보이는 경우가 있으나, 세포의 증식과 관련된 Ki-67 염색에 있어서는 단핵구에서만 양성을 보이고 있어 단핵구가 거대세포육아종의 주요 증식 성분으로 인식되고 있다[2,3]. 본 증례의 경우 Ki-67 염색에 1% 미만의 비특이적 반응을 보여 병변의 증식도가 높지 않았을 것으로 생각된다.
말초 거대세포육아종은 중심 거대세포육아종, 거대세포종(Giant cell tumor), 비골화성 섬유종(Non-ossifying fibroma), 화농성 육아종(Pyogenic granuloma), 부갑상샘항진증에서 보이는 갈색종양(Brown tumor) 등과의 감별이 필요하다[6,13]. 말초 거대세포육아종이 진행할 경우 골흡수를 통해 골 내부로 침범하는 경우가 있어, 골 내에서 시작된 중심 거대세포육아종이 피질골 밖으로 진행한 것인지 구별이 어려울 수 있으나 컵모양 골흡수(“Cupping” resorption) 등의 영상학적인 특징으로 감별하기도 한다. 거대세포종의 경우 악골에 호발하는 거대세포육아종과 달리 주로 장골에 호발하고, 거대세포육아종에 비해 더많은 수의 핵을 가진 더 큰 크기의 거대세포가 더 많은 숫자로 종양 조직 전반에 걸쳐 균일하게 분포하며 출혈 소견 주변으로의 유골 생성이 드물다. 비골화성 섬유종은 대부분 장골의 골간단부위에 호발하고 조직병리학적으로 방추상의 섬유모세포가 특징적인 소용돌이 배열을 보여 감별할 수 있고, 화농성 육아종의 경우 임상소견이 매우 유사하나 조직병리학적으로 거대세포육아종에 비해 골흡수 경향이 적고, 모세혈관이 현저하게 증식된 양상을 보여 감별이 가능하다. 갈색종의 경우 조직병리학적 검사로는 감별이 어려우므로 혈액검사에서 나타나는 부갑상샘 항진증 소견으로 감별한다.
거대세포육아종의 치료는 수술적 절제로, 재발의 방지를 위해 부착하고 있거나 침범한 골 및 골막은 반드시 포함하여 절제하는 것을 원칙으로 한다. 본 증례의 경우 수술 전 와르틴 종양 의심하에 병변을 포함한 주변 이하선 조직을 함께 절제하는 이하선 부분절제술을 시행하였으며 병변이 골 및 골막과의 관계 없이 고립된 종괴를 형성하고 있어 완전한 절제가 가능하였다.
말초 거대세포종의 경우 임상적 소견이나 영상학적 소견의 유사성을 보이는 다양한 질환들이 있고, 예후, 재발경향성, 악성화, 치료 등에 있어 차이를 보이므로 감별진단이 필수적이나, 수술적 절제 후 조직병리학적 검사를 통해서만 확진이 가능하므로, 호발 부위가 아닌 다른 부위에서 발생한 경우 거대세포종을 의심하기가 어렵다는 문제가 있다. 본 증례의 경우에도 골 침범을 보이지 않고 이하선에 단독으로 발생하여 세침 흡인검사에서 거대세포가 발견되었음에도 말초 거대세포종을 고려하지 못하였고, 수술 후 시행한 조직병리학적 검사를 통해 확진하였다. 본 증례의 경우 고립된 종괴의 완전한 절제를 시행하였고 말초 거대세포종의 경우 완전 절제 시 재발경향성이 낮아 1년 후 경부 컴퓨터단층촬영을 통한 추적 검사 예정이다.