서론
2019 미국 임상종양학회(American Society of Clinical Oncology, 이하 ASCO)는 2019년 5월 31일 부터 6월 4일까지 예년과 같이 미국 시카고에서 개최되었다. ‘Caring for Every Patient, Learning from Every Patient’라는 테마로 열린 2019 ASCO에는 전세계에서 32,000명이 넘는 종양학 전문가들이 참여하였다. 전체적으로 약 2400개가 넘는 초록이 발표되었으며, 이 중 두경부암 분야에서는 8개의 구연발표와 75개의 포스터 발표가 있었다. 여기서는 구연으로 발표된 8개의 연구를 중심으로 정리해 보고자 한다.
본론
Abstract 6000: Protocol-specified final analysis of the phase 3 KEYNOTE-048 trial of Pembrolizumab (Pembro) as first-line therapy for recurrent/metastatic head and neck squamous cell carcinoma (R/M HNSCC)
현재 재발성/전이성 두경부편평상피세포암의 현재 표준치료는 ‘Cetuximab + 5-FU + platinum’이며 이는 Vermorken 등이 2008년 NEJM에 발표한 EXTREME 연구를 근거로 한다[1]. EXTREME 연구는 재발성/전이성 두경부편평상피세포암의 1차 항암치료로 기존 세포독성 항암치료(5-FU + platinum)에 항 EGFR 단클론 항체인 Cetuximab을 추가하여 전체 생존 기간을 7.4개월에서 10.1개월로 향상(Hazard ratio = 0.80, p-value = 0.04) 시킨 연구이다. 현재 우리나라에서는 아직 Cetuximab의 보험급여가 되지 않고 있지 않지만 외국에서 재발성/전이성 두경부편평상피세포암의 1차 표준항암치료는 ‘Cetuximab + 5-FU + platinum’이며, EXTREME 연구에서 나온 용법이라 해서 EXTREME 용법이라고도 불린다.
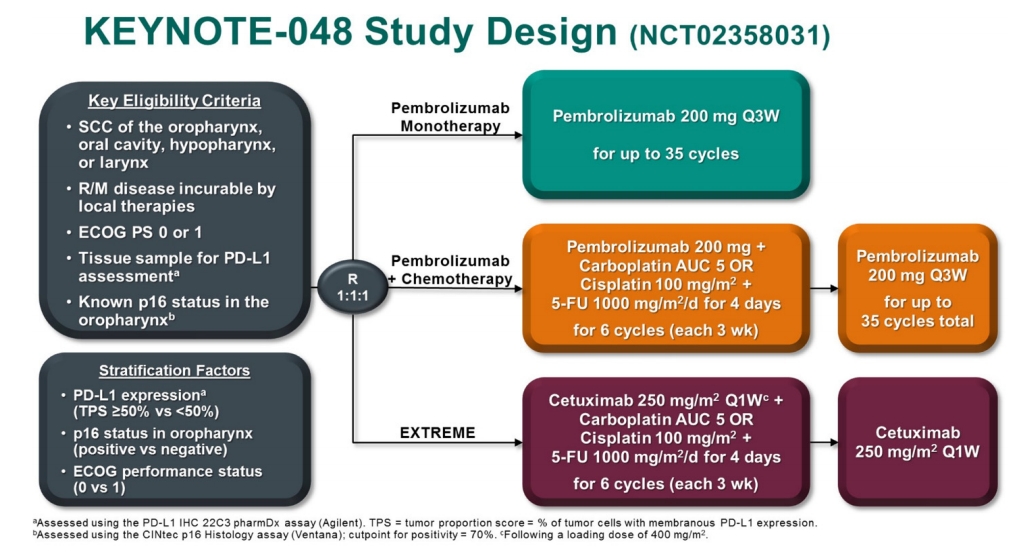
KEYNOTE-048 연구는 재발성/전이성 두경부편평상피세포암에서 현재 표준 치료인 EXTREME 용법(Cetuximab + 5-FU + platinum)에 비해서 Pembrolizumab (P) 또는 Pembrolizumab + chemotherapy (5-FU + platinum; P + C)의 성적을 비교한 3상 무작위배정 임상연구이다(Fig. 1). Rischin 등은 2018 ESMO에서 KEYNOTE-048연구의 중간 분석을 발표한 후 이번 ASCO에서 프로토콜에 명시된 최종 분석결과를 발표하였다[2].
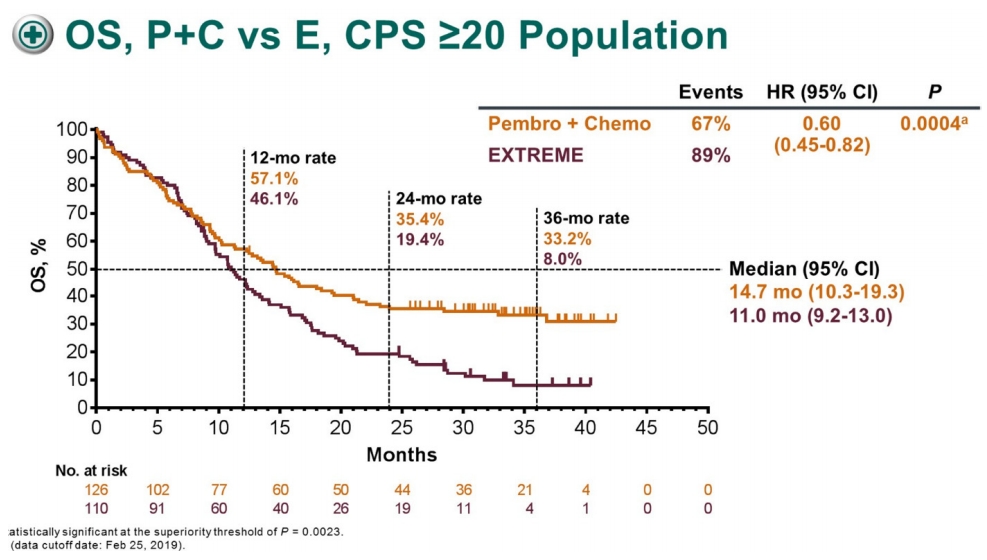
총882명의 환자를 P 단독(200 mg 3주간격, 24개월), P + C (P 24개월 + chemotherapy (5-FU + platinum) 6주기), 또는 EXTREME 용법에 1:1:1로 무작위 배정하였다. PD-L1 복합 양성 수치(PD-L1 combined positive score: CPS)를 기준으로 20이상, 1 이상에서 P + C 와 EXTREME 군의 생존기간을 비교하였고, 전체 환자군에서 P 대 EXTREME 군의 생존기간의 우월성을 분석하였다. 결론적으로 P + C 군이 EXTREME 군보다 CPS ≥ 20일때 중앙생존기간(Median OS), 14.7 vs 11.0 개월(HR 0.60, 95% CI 0.45-0.82, P = 0.0004)(Fig. 2), CPS ≥ 1일때도 중앙생존기간 13.6 vs 10.4 개월(HR 0.65, 95% CI 0.53-0.80, P < 0.0001)으로 P + C 군이 더 우월한 생존기간을 보여주었다. 전체 환자군에서 P 대 EXTREME 간의 비교는 중앙생존기간 11.5 vs 10.7 개월(HR 0.83, 95% CI 0.70-0.99, P = 0.0199)으로 통계적으로 P단독 군이 EXTREME 군에 비해 우월함(Superiority)을 보여주지는 못하였다. 3등급(Grade 3) 이상의 독성면에서는 각각 P 단독 군이 54.7%, P+C 군이 85.1%, EXTREME 군이 83.3% 였다.
이 연구의 의의는 재발성/전이성 두경부편평상피세포암 환자에서 기본(Backbone)으로 사용하는 5-FU + platinum에 Cetuximab 보다는 면역관문억제제인 Pembrolizumab의 병합용법이 우월한 것임을 보여 준 것이다. 이번 연구 결과를 바탕으로 향후 고식적 1차 항암치료의 표준치료 용법이 바뀔 것으로 예상이 된다(Clinical trial information: NCT02358031).
Abstract 6001: Ado-trastuzumab emtansine in patients with HER2 amplified salivary gland cancers (SGCs): Results from a phase II basket trial
MSK-IMPACT (Memorial Sloan Kettering-Integrated Mutation Profiling of Actionable Cancer Targets) 데이터를 보면 HER-2 증폭(Amplification)을 보이는 고형암은 위암, 유방암, 침샘암 순이다. 모든 침샘암 환자의 약 8%에서 HER-2 증폭을 보인다고 알려져 있는데, 공격적인(aggressive) 침샘암의 경우 25-33%의 환자에서 HER-2 증폭이 있다고 알려져 있다[3].
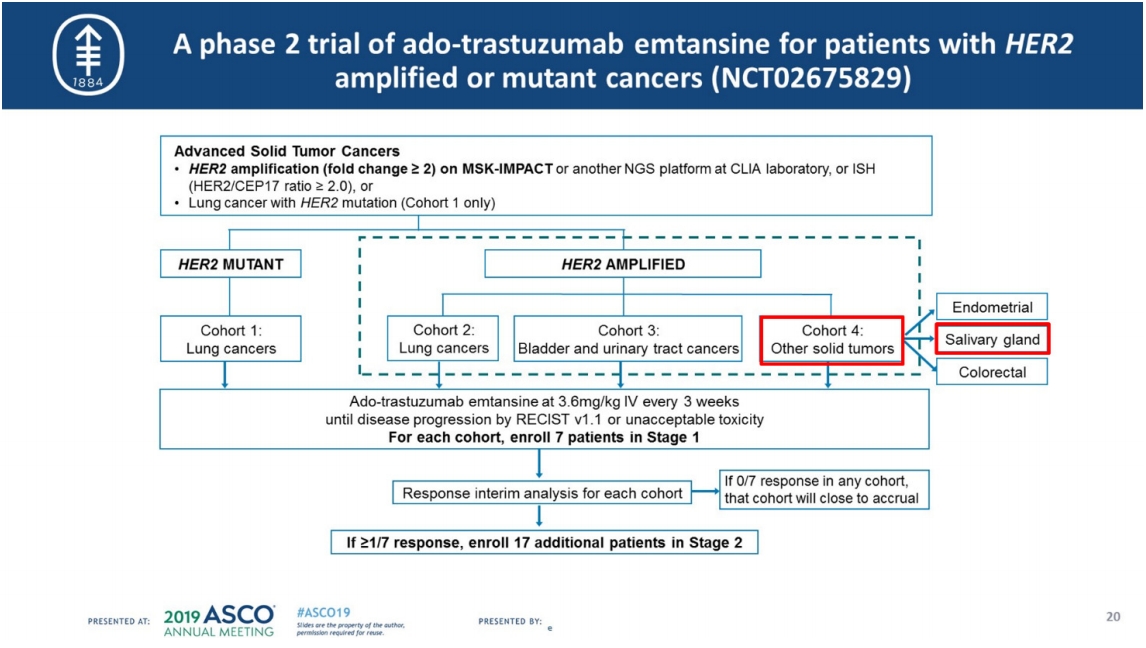
Bob T. Li 등의 Memorial Sloan Kettering Cancer Center 연구자들은 HER-2 증폭 또는 돌연변이가 있는 고형암에서 Ado-trastuzumab emtansine (T-DM1)을 사용하는 2상 바구니 임상연구(Phase 2 basket trial)을 진행하고 있다(Fig. 3)(NCT02675829).
이 중 Cohort 4 (기타 고형암)에서 치료받은 10명의 HER-2 증폭 침샘암(HER-2 amplified salivary gland cancers)의 2상 임상연구 결과를 2019 ASCO에서 발표하였다[4]. 주된 연구 목표(Primary endpoint)는 전체 반응률(Overall response rate)이였는데 10명의 등록 환자 중 9명이 부분 반응 이상을 보여 반응률 90%의 놀라운 성적을 보여주었다. 반응시간도 길어서 12개월 추적관찰 기간동안 중앙 반응 기간 및 무진행 생존기간이 중간값에 도달하지 않는 우수한 성적을 보여주었다. HER2 증폭의 판별은 차세대유전체분석(Next Generation Sequencing: NGS)으로 스크리닝하고, 이후 FISH 와 IHC로 확인하였다. NGS로 확인한 HER2 증폭(fold change 2.8 to 22.8)은 FISH (HER2/CEP17 ≥ 2)와 IHC 3+ 와 정확하게 연관성을 보여주었다고 보고하였다. 아직 등록 환자수가 적긴 하지만 차세대유전체분석을 활용한 표적 확인과 적절한 치료제를 적용함으로써, 임상적 유용성을 증명한 우수한 연구결과라고 할 수 있겠다. 다만 아직 등록 환자가 수가 적은 점을 고려한다면 추후 코호트 확장 등을 통한 보다 많은 환자들에게서 검증이 되어야 할 것이다.
Abstract 6002: TPExtreme randomized trial: TPEx versus Extreme regimen in 1st line recurrent/meta-static head and neck squamous cell carcinoma (R/M HNSCC)
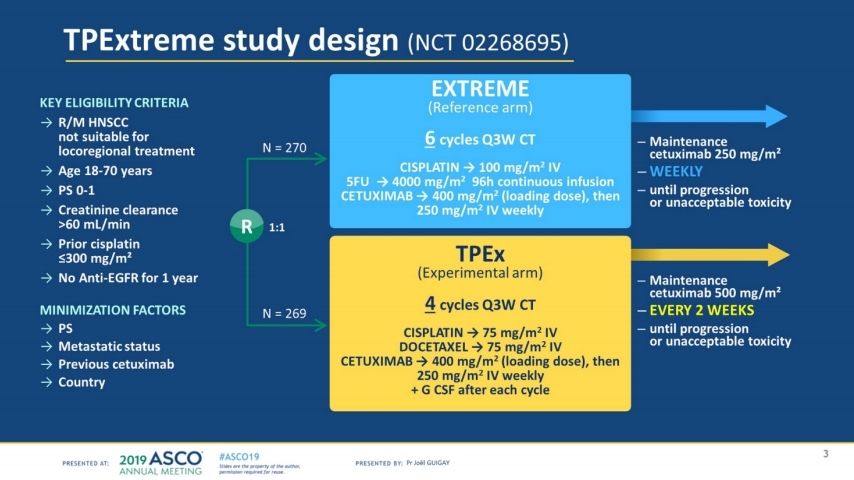
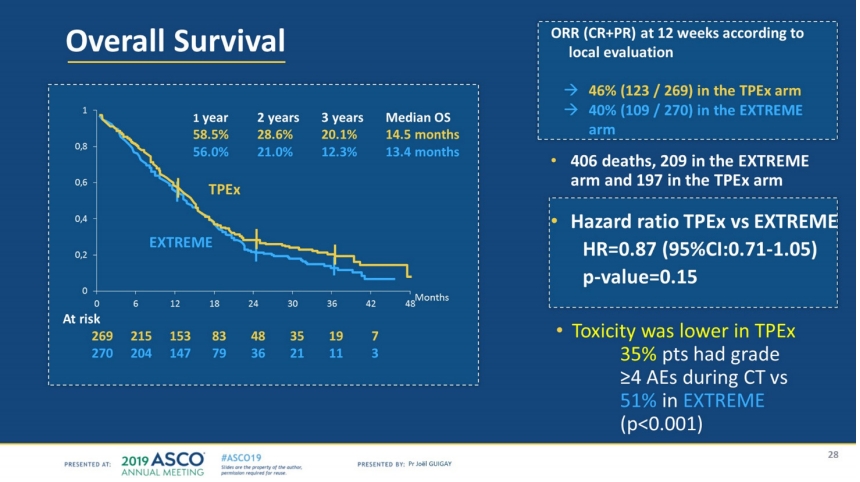
GUIGAY 등은 GORTEC의 TPExtreme 연구결과를 발표하였는데 이 연구는 EXTREME 용법(Cetuximab + 5-FU + platinum)에서 5-FU 대신 Docetaxel을 사용하여 Taxane을 기반으로 한 TPEx 용법(Docetaxel + platinum + cetuximab)이 EXTREME 용법보다 항암치료를 적게(EXTREME 용법은 6 주기, Taxane 기반 TPEx 용법은 4 주기)하고도 부작용은 적으면서, 효과는 더 나을 것이다는 가정 하에 진행되었다(Fig. 4)(NCT02268695) [5,6].
총 539명이 EXTREME 용법과 Taxane 기반 TPEx용법으로 각각 1:1로 부작위 배정되었고, 1차 연구 목적으로 생존율을 비교 하였다. 생존율 비교에서(30개월 중앙 추적관찰 기간) Taxane 기반 TPEx용법 군의 중앙 생존기간은 14.6개월, Extreme 용법 군은 13.4개월로 통계학적으로 유의한 차이를 보여주지는 못하였다(HR=0.87, 95%CI: 0.71-1.05, p=0.15)(Fig. 5). 부작용 측면에서는 4등급 이상의 부작용의 경우 Taxane 기반 TPEx군에서는 34%, EXTREME 용법 군에서는 50%였다(p<0.001). 유지요법의 경우 Taxane 기반 TPEx 용법군에서는 73%가, EXTREME 용법 군에서는 53%에서만 시작할 수 있었다. 해당 연구가 주요 연구목적을 만족시키지 못했는데, 그 이유는 연구 참여자의 약 1/4이 2차 이상 항암치료로 면역항암제를 투여 받았고 이로 인해 생존기간의 늘어나면서 이번 연구 결과에 일정 부분 영향을 주었다고 해석해 볼 수 있겠다.
이번 연구의 결과로 Taxane 기반 TPEx용법이 현재 표준치료인 EXTREME 용법을 대체하지는 못할 것으로 보인다. 이미 1차 항암치료시에 5-FU대신 Taxane계열 약제로 바꾸어서 사용하는 경우가 많기 때문이다. 다만 5-FU가 펌프 등을 사용해야 하는 투약 과정상의 불편함이 있기에 이를 대신할 정도의 역할을 할 것으로 예상할 수 있겠다.
Abstract 6003: Gemcitabine and cisplatin (GP) induction chemotherapy (IC) plus concurrent chemoradiotherapy (CCRT) versus CCRT alone in locoregionally advanced nasopharyngeal carcinoma (NPC): A phase 3, multicenter, randomized controlled trial
Abstract 6004: Induction chemotherapy followed by concurrent chemoradiotherapy versus concurrent chemoradiotherapy alone in locoregionally advanced nasopharyngeal carcinoma: Long-term results of a phase 3 multicenter randomized controlled trial
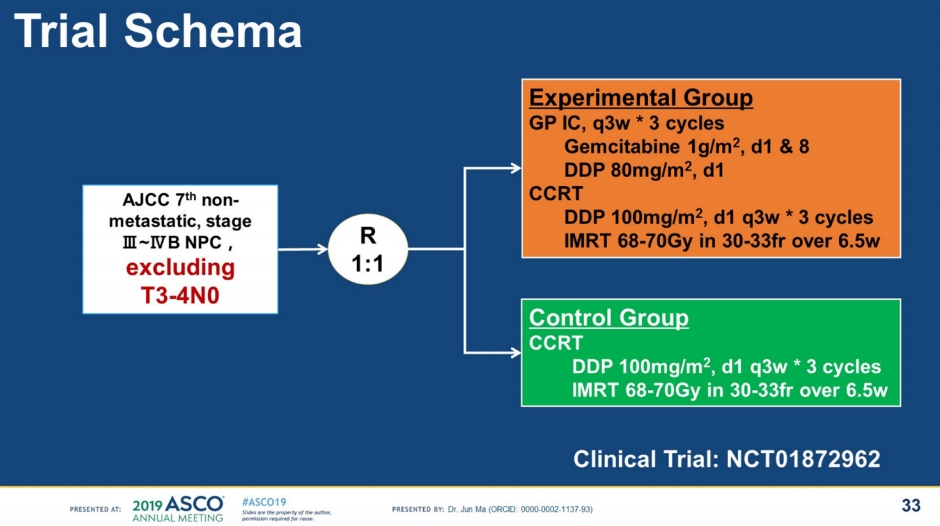
#6003, #6004 두 개의 연구는 국소 진행성 비인두암(locally advanced nasopharyngeal carcinoma; NPC)에서 유도항암치료(induction chemotherapy)에 대한 연구이다. 국소 진행성 비인두암의 현재 표준은 동시항암방사선치료(CCRT) 이후 +/- 보조 항암치료이다. #6003에서는 Gemcitabine / Cisplatin (GP: gemcitabine 1 g/m2on days 1 & 8, cisplatin 80 mg/m2 on day 1, 3주간격, 3주기)로 유도항암치료를 하고 동시항암방사선치료(cisplatin 100 mg/m2, 3주간격, 3주기, 세기 조절 방사선치료(intensity-modulated radiotherapy: IMRT)와 함께)를 하였고(Fig. 6) [7], #6004에서는 유도 항암치료로 PF (cisplatin (80 mg/m2 d1) and fluorouracil (800 mg/m2 d1-5))을 2주기하고 동시항암방사선치료(80 mg/m2 cisplatin every three weeks + RT)를 진행하였다[8].
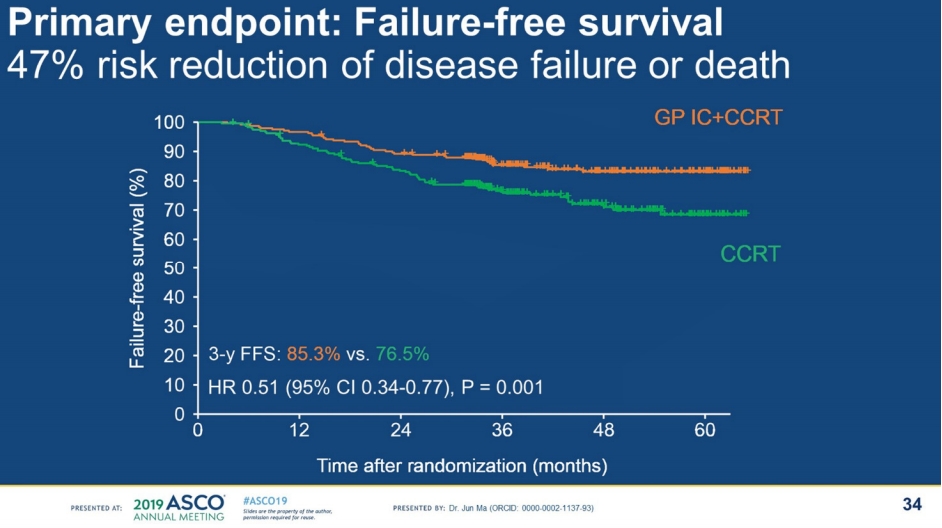
#6003에서는 1차연구 목표가 무실패 생존기간(Failure-free survival: FFS) 이었는데 3년 무실패 생존기간이 유도항암치료 후 동시항암방사선치료 군(IC+CCRT group)에서 85.8%, 동시항암방사선치료 군에서 77.2% (Intention to treat population; HR 0.53, 95% CI 0.34-0.81; P = 0.003)으로 통계적으로 유의한 성적 향상을 보여주었다(Fig. 7).
#6004에서도 5년 무병생존율(Disease-free survival: DFS)을 유도항암치료 후 동시항암방사선치료 군 73.4% 대 동시항암방사선치료 군 63.1%으로 통계학적으로 유의한(P = 0.005) 성적을 보고 하였다. 또한 5년 무원격전이 생존율(Distant metastasis-free survival: DMFS) 및 5년 생존율에서도 유도항암치료 후 동시항암방사선치료 군(IC+CCRT group)이 동시항암방사선치료 군(CCRT group)에 비해서 유의한 성적 향상을 보고하였다.
두개의 연구를 종합해 보면 국소 진행성 비인두암에서 유도항암치료 후 동시항암방사선치료를 하는 것이 성적을 향상시킨다는 것을 알 수 있겠다. 물론 항암치료에 따른 독성을 감내해야 하겠지만 환자 선택을 잘 한다면 큰 문제가 되지 않을 것으로 예상해 볼 수 있다. 두개의 연구 결과로 유도항암치료 후 동시항암방사선치료가 NCCN 진료지침에서도 카테고리 3에서 2A로 올라갔다. 또한 유도항암치료 용법으로는 GP (Gemcitabine/Cisplatin)가 좀 더 원만할 것으로 생각된다. 하지만 아직 우리나라에서는 1차 치료 실패 상태에서 GP 용법의 사용도 아직 보험 급여가 되지 않아 사전 급여 신청으로 100% 환자 본인부담으로만 사용 가능하다. 이러한 현실로 미루어 보았을 때 실제 임상현장으로 들어오기 까지는 좀 더 시간이 걸릴 것으로 예상된다.
Abstract 6006: A phase II randomized trial for early-stage squamous cell carcinoma of the oropharynx: Radiotherapy versus trans-oral robotic surgery (ORATOR)
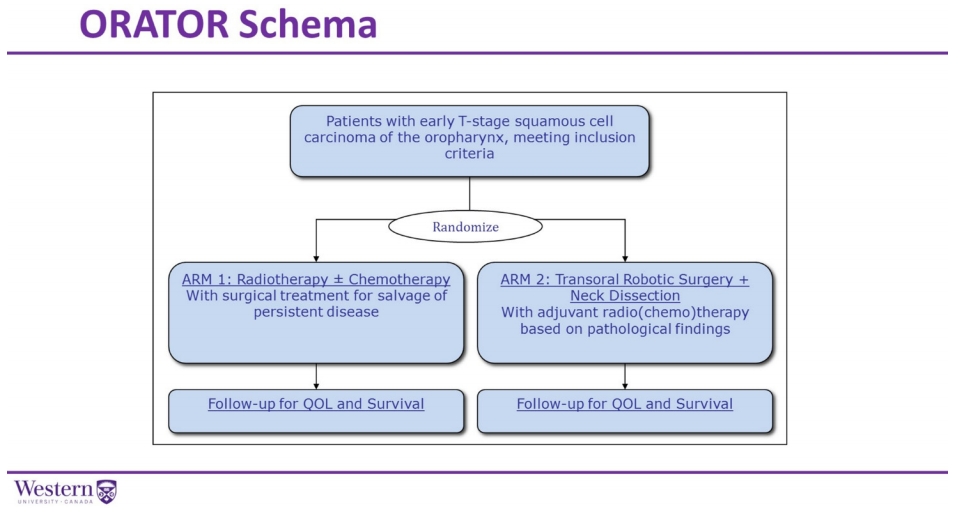
A. Nichols 등 Canada Cancer Society 연구자들은 초기 구인두 상피세포암(early stage oropharyngeal squmous cell carcinoma; OPSCC)에서 방사선치료와 경구강 로봇수술(Trans-oral robotic surgery: TORS)를 비교한 2상 임상연구 결과(ORATOR 연구)를 발표하였다(Fig. 8) [9].
구인두암은 인간 유두종 바이러스(Human Papilloma Virus: HPV) 감염으로 최근 급격하게 늘고 있다. 원래 구인두암의 경우 전통적으로 방사선치료가 주된 치료법인데, 최근 로봇을 사용한 경구강 로봇 수술이 독성을 줄이고 삶의 질을 높힐 것이라는 믿음 하에 방사선치료 보다 더 자주 적용되고 있다고 한다. 하지만 방사선치료 보다 경구강 로봇 수술이 더 우수하다는 직접적인 증거가 없기 때문에, 이에 대한 근거를 확인해 보고자 이 연구가 기획되었다고 한다. 일견 실행 불가능해 보이는 두 치료 방법 간의 전향적 비교연구는, 이비인후과와 방사선종양학과교수가 직접 주요 연구자로 참여하여 연구가 실현되었다.
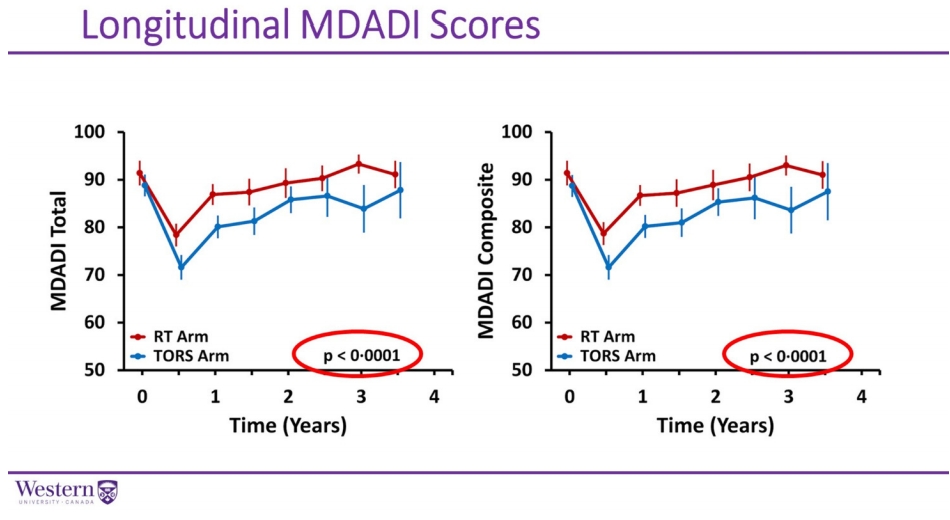
연구는 T1-T2 N0-2 (≤4 cm) 초기 구인두 상피세포암으로 진단되어 경구강 로봇 수술이 가능한 환자 68명을 방사선 치료와 경구강 로봇 수술로 1:1 무작위 배정하여 1년 시점에서 삼킴 질 검사 결과(Swallowing Quality of Life, 지표는 The M. D. Anderson Dysphagia Inventory: MDADI을 사용함)를 비교하였다. 중앙 추적관찰기간 27개월이 지난 시점에서 연구 주요 목적인 삼킴 질 지표인 MDADI 비교에서 방사선치료 군이 경구강 로봇 수술군보다 통계학적으로 우월한 성적을 보여주었다(Fig. 9). 하지만 이러한 통계학적 차이가 임상적으로는 유의한 차이가 아니었다고 평가하였다.
생존기간, 무진행 생존기간 모두 두 군 간의 차이는 없었다. 따라서 조심스럽기는 하지만 초기 구인두 상피세포암에서 방사선치료가 삼킴 질 측면에서 경구강 로봇수술보다 더 우월하였다고 할 수 있겠다. ORTOR연구는 초기 구인두 상피세포암에서 방사선치료와 수술적 방법을 비교한 첫번째 전향적 무작위 배정 연구로 상당한 의미가 있는 연구라고 할 수 있다. 향후 본 연구 결과를 뒷받침할 만한 후속 연구를 기다려 볼 필요가 있겠다.
Abstract 6007: Neck dissections based on sentinel lymph node navigation versus elective neck dissections in early oral cancers: A randomized, multicenter, non-inferiority trial
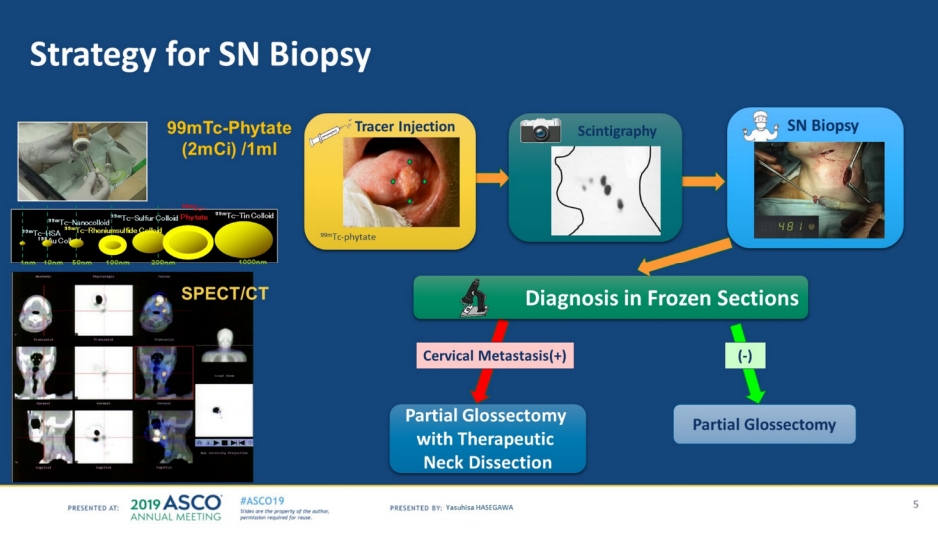
현재 초기 구강 내 편평상피세포암(Early stage oral squamous cell cancer)에서 수술 시 선택적 경부 임파선 절제(Elective neck lymph node dissection)를 하는 것이 표준치료이다[10]. 하지만 모든 환자에게 광범이 경부 임파선 절제를 하는 것은 여러가지 부작용 및 합병증을 수반할 수밖에 없다. 따라서 유방암 수술시와 마찬가지로 감시 임파선 탐색(Sentinel LN navigation)을 통해 경부 임파선 절제 여부를 결정함으로써 수술 후 장애, 합병증을 줄일 수 있지 않을까 하는 가정에서 연구가 설계되었다(Fig. 10) [11].
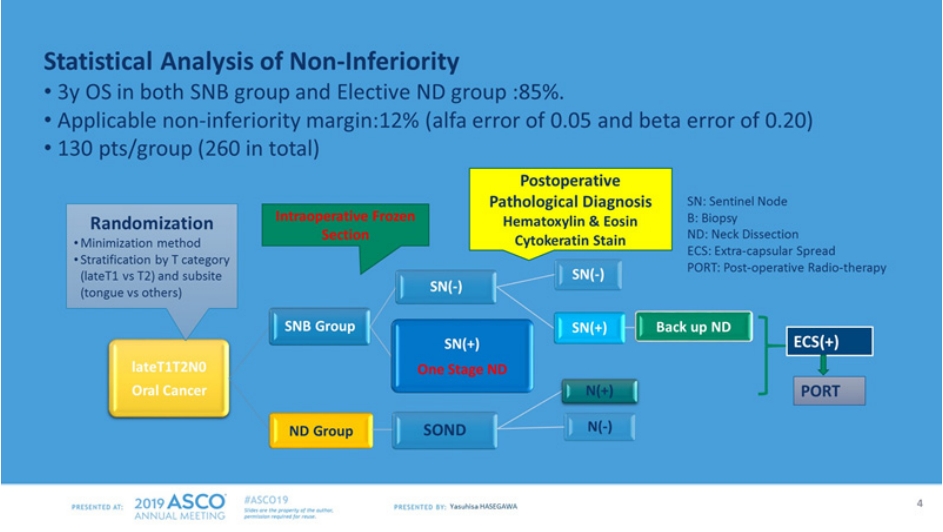
Y. Hasegawa 등은 cT1/2 N0M0 환자 271명을 감시 임파선 탐색 후 절제군(SND group) 134명, 선택적 임파선 절제군(ND group) 137명으로 1:1 무작위 배정하여 3년 생존율을 비교하고자 하였다(비열등성 임상시험: Non-inferiority study)(Fig. 11).
3년 생존율은 감시 임파선 탐색 후 절제군이 89%, 선택적 임파선 절제군이 86%으로 비열등성을 보여주었고(P = 0.5027), 3년 무재발 생존율 또한 두 군 간에 차이가 없었다(P = 0.4047). 수술 후 1, 3개월시점에서 팔 외전검사(Arm abduction test)에서는 선택적 임파선 절제군이 감시 임파선 탐색 후 절제군보다 더 심하게 불편함을 겪었다. 따라서 감시 임파선 탐색 후 절제가 생존율에 영향을 주지 않으면서 선택적 임파선 절제를 대치할 수 있을 것이라는 의견을 제시하였다. 효능에 영향을 주지 않으면서 독성을 줄이는 임상적으로 의미가 큰 연구라고 생각된다.
Abstract 6008 Checkpoint inhibitors assessment in oropharynx cancer (CIAO): Safety and interim results
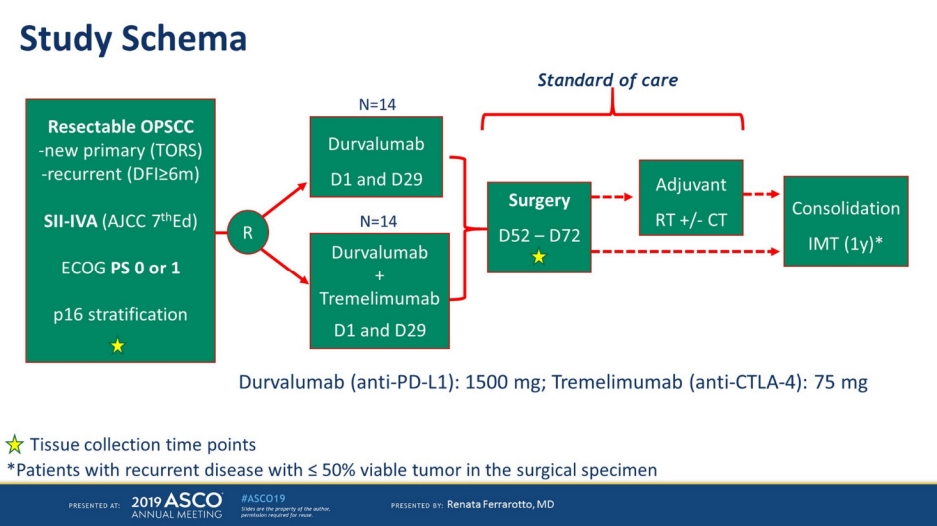
본 연구는 구인두암의 수술적 치료 전 선행 면역관문억제제로 항 PD-L1 억제제인 Durvalumab (Durva 1500 mg IV, 4주간격 2주기) 또는 Durvalumab + Tremelimumab (Durva 1500 mg + Treme 75 mg IV 4주간격 2주기)을 사용하여 각 군에서 투약 전 후 CD8 양성 종양 침투 림프구(CD8+ tumor infiltrating lymphocytes: TIL)을 비교하고자 하는 연구이다(Fig. 12). 면역관문억제제가 획득 면역반응을 유도한다면 투약 전 CD8+ TIL에 비해서 투약 후 CD8+ TIL이 유의하게 증가하지 않을까 하는 가정에서 연구가 진행되었다. 물론 2차 연구 목적으로 안정성, 독성, 종양 반응률 등이 포함되어 있다[12].
총 28명의 환자(63%가 4기A)가 등록된 연구에서 전체반응률은 Durvalumab 43%, Durva + Treme 43%로 Tremelimumab의 병합투여 여부가 임상적인 차이를 보여 주지는 못하였다(Fig. 13).
주요 임상연구 목적 이였던 치료 전 후 CD8 TIL의 비(ratio)의 경우 Durva 군 1.43, Durva + Treme 군 1.12을 보여주었다(즉 Durva군의 경우 투여 전에 비해서 2주기의 Durvalumab 투여 후 수술 병리 검사에서 CD8 TIL이 43% 정도 늘어남). 특히 32%에서 주요 병리학적 반응(Major pathologic response: mPR) 보여주었는데 mPR을 보여주었던 환자의 경우, 치료 전 후 CD8 TIL의 비(ratio)가 3.5까지 상승하였다. 따라서 수술 전 면역관문억제제 투약을 통해 면역반응을 유발할 수 있다면, 수술 성적을 향상시킬 수 있다는 것을 보여주었다. 이러한 수술 전 면역관문억제제가 폐암 등 다양한 암종에서 연구되고 있는 만큼 향후 대규모 연구 결과가 기다려 진다.
결론
미국 임상 종양 학회 2019년 연례 회의에는 작년과 마찬가지로 임상적으로 중요한 연구 결과들이 다수 발표되었다. 재발성 또는 전이성 두경부편평상피암에서 1차 치료의 역할로서 면역관문억제제인 Pembrolizumab과의 병용용법이 기존 표준 치료에 비해 우수한 성적을 보여주어, 두경부편평상피암의 1차치료에 면역관문억제제의 사용이 보편화 될 것으로 예측해 볼 수 있다(NCT02358031). 난치성 침샘암의 경우 기존 세포 독성 항암치료에 잘 반응하지 않아 성적이 좋지 않지만, HER-2 증폭이 있는 경우 표적치료제인 T-DM1에 대한 반응이 우수 할 것이라는 연구는 두경부암에서도 정밀의료가 가능하다는 메시지를 줄 수 있는 연구이다(NCT02675829). 국소진행성 비인두암의 경우 우리나라에는 발생 빈도가 높지 않은 암이다. 비인두암은 여타암과 비슷하게 1차 표준치료 후 재발하게 되면 치료 옵션이 매우 제한적이다. 따라서 1차 치료의 역할이 매우 중요한데 이번 발표에서 유도항암치료를 사용함으로써 성적 향상을 보여주었고, 곧장 임상에도 적용할 수 있을 것으로 예상할 수 있겠다(NCT01872962). ORATOR 연구는 구인두암에서 수술 위주의 치료 방법에 비해 방사선치료도 비슷한(합병증 측면에서는 조금 나은) 치료법임을 증명해 보였고(NCT01590355), 구강암에서 감시 임파선 탐색 연구는 수술이 필요한 환자를 적절히 선택하여 불필요한 수술을 줄이고자 하는 바람직한 방향을 제시해 준 매우 의미 있는 연구라고 할 수 있다(NCT000006510). 향후 두경부암 분야에도 발전적인 연구가 계속되기를 기대해 본다.